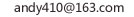中考化学题,求详细解答
猜想2,应该写(NH4)2SO4,题目中已经说明只有一瓶药品
(1)中考查的是NH4+离子的检验。当NH4+遇到OH-的时候,会有NH3气体产生,所以会有刺激性气味。故猜想4不正确,尿素中没有铵根离子。
余下三种物质都有铵根离子,但是阴离子不同,分别是氯离子,硫酸根离子,碳酸氢根离子。三种离子中,只有碳酸氢根离子遇到H+的时候会产生气体。根据题意,应该是猜想三不正确,加入的是盐酸,是第三瓶吧
(3)中考查氯离子和硫酸根离子的不同检验。如果图2中间那瓶是氯化钡的话(实在看不清啊,。。),则没有产生沉淀时猜想一正确,有产生沉淀时猜想二正确。BaCl2+(NH4)2SO4=BaSO4(沉淀符号)+2NH4Cl。
希望对你有所帮助。
初三化学,应用题。求详细解答过程。
答:分析:(1)欲正确解答本题,需根据化学方程式得出各物质之间的质量比,列出比例式,通过计算得出所需物质的质量.然后根据溶质质量分数公式计算即可.(2)根据已知条件计算出合格奶粉中氮元素的质量分数范围,再与该奶粉中的含氮元素的质量分数比较即可.解答:解:(1)设产生氨气的质量为x,2NH3+H2SO...
初三化学题 求大神给详细过程 拜托啦~会加分的。
答:故答案为:(1)1200克;(2)吸收相同质量的二氧化碳所需氢氧化锂的质量小,可以减轻火箭发射的重量.注意:本题容易出错的地方是单位换算,体积不能带入方程式计算,必须换算成质量.
初三化学题 求解答
答:(1)从生成物分析,该有机化合物一定含有( 碳和氢 )元素,可能含有( 氧 )元素。(2)今将9.6g该有机物完全燃烧后,生成水的质量是10.8g,生成二氧化碳的质量为13.2g,计算该9.6g有机物中含有哪几种元素?各多少克?含碳 13.2g*12/44=3.6g 含氢 10.8g*2/18=1.2g 含氧 ...
一道初三化学题,求详细解析。
答:说明固体中一定有排在氢前的金属,而Zn+CuCl2=Cu+ZnCl2,Zn+FeCl2=Fe+ZnCl2,Fe+CuCl2=Cu+FeCl2,反应顺序是首先Zn置换出Cu,然后Zn置换出Fe,因滤渣与稀盐酸产生气体,故一定有Cu,至少还有Fe,可能还有Zn.由此分析,一定含有Cu、Fe.所以,选A 不懂的欢迎追问,如有帮助请及时采纳,谢谢!
化学中考题急急
答:由CaCO3+CO2+H2O=Ca(HCO3)2可知,Na2CO3溶液与CO2发生化学反应的化学方程式是:Na2CO3+CO2+H2O═2NaHCO3;依据此化学反应的规律,碳酸钾溶液与二氧化碳反应方程式是:K2CO3+CO2+H2O═2KHCO3;故答案为:CaCl2;有沉淀生成;既有气体又有沉淀生成;Na2CO3+CO2+H2O═2NaHCO3;K2CO3+CO2+H2O═2KHCO3...
初三化学。高分赏
答:1.首先,因为氯化氢气体的体积为3.36L.因为标况下,每摩尔气体的体积为22.4L.说明氯化氢的物质的量3.36/22.4=0.15摩尔.因为配成了500mL溶液,则可知溶液的浓度为0.15/0.5=0.3mol/L.因此溶液的物质的量为0.3mol/L.2.根据题中的意思,可知需要CuSO4.5H2O的物质的量为0.5*0.2=0.1摩尔...
初三化学选择题(答案已给出,求详细讲解)
答:解释:CuO + H2SO4 = CuSO4 + H2O、Fe + H2SO4 = FeSO4 + H2↑、Fe + CuSO4 = FeSO4 + Cu。插入锌片有气泡产生是因为Zn + H2SO4 = ZnSO4 + H2↑,说明硫酸有剩余,则Fe不存在,剩余固体一定只有铜。2、将下列物质的溶液分别滴入到氯化钙溶液、氢氧化钠溶液和稀硫酸中,能观察到三种...
几道初三化学题,求解答
答:2、第一题:物质燃烧生成二氧化碳和水,根据质量守恒定律,反应前后元素种类不变,所以一定含有碳、氢元素,可能含有氧元素。第二题:计算确定是否含有氧元素 生成了3.6gH2O所以反应前氢元素质量也为3.6/18*2=0.4g 同理8.8g二氧化碳计算得C的质量为8.8/44*12=2.4g 所以一定含有O,O的质量为3....
一道中考化学题 求详细解析 越详细越好 可追加分
答:分析:因为铝的相对原子质量比铁、锌都小,所以相同质量的铝与盐酸完全反应时,产生的氢气质量多.解答:解:假设合金中铁的质量为5.6 g,则根据化学反应的方程式:Fe+2HCl=FeCl2+H2↑可计算出此时产生氢气的质量为0.2 g,同理可计算出5.6 gAl与足量盐酸反应产生氢气的质量大于0.2 g,5.6gZn与...
一道初三化学计算题,写出讲解和步骤!
答:初三化学计算题,求解答步骤 解:设溶质的质量为x NaCl + AgNO3 → NaNO3+ AgCl ↓ 85 143 x 28.7g 85/x=143/28.7g 解得x=17.06g 溶质NaNO3的质量分数为17.06÷(70+100-28.7)×100%=12.1 一道初三化学计算题 1 16/32*100%=50% 2 含有0.32%甲醇的工业废水500t...